季節の変わり目に注意!咳・喘息・アレルギー症状の原因と対処法【おきのメディカル(仙台市)】

季節の変わり目に呼吸器症状が増えるのはなぜ?
宮城県仙台市では、春先や秋口など季節の変わり目に気温や湿度の変化が大きく、咳や鼻炎、喘息などの呼吸器症状でご来院される患者様が増加します。
「咳が長引く」「朝方に息苦しさを感じる」「鼻水やくしゃみが止まらない」などの症状は、風邪だけでなく、咳喘息やアレルギー、気管支喘息などの疾患が背景にある可能性もあります。
呼吸器内科・内科に受診する必要があるか?―具体的な疾患と治療法
以下のような症状が見られる方は疾患を患っている可能性があり、内科や呼吸器内科などを受診することをおすすめします。
| 症状 | 考えられる疾患 |
|---|---|
| 咳が3週間以上続く | 咳喘息、感染後咳嗽、アトピー咳嗽 |
| 息をするたびにヒューヒュー・ゼーゼー音がする | 気管支喘息、COPD |
| 鼻水やくしゃみ、目のかゆみ | アレルギー性鼻炎、花粉症 |
▼これらの疾患に関して具体的に解説していきます
咳喘息
・空咳(痰を伴わない咳)が8週間以上続く
- ・喘鳴や呼吸困難はなく、風邪後に出やすい
治療法:
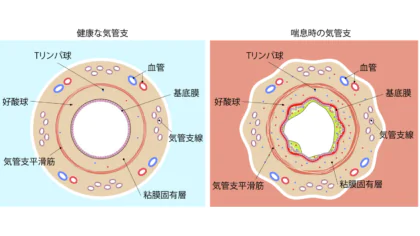
喘息は気道が慢性的に炎症を起こし、さまざまな刺激に対して過敏に反応することで、咳を主症状となる病気です。咳喘息の治療では、まず吸入ステロイド薬(ICS)を使用し、気道の慢性的な炎症を抑えることが基本となります。代表的な薬剤には、アニュイティ®、パルミコート®、オルベスコ®などがあり、これらを毎日継続的に吸入することで症状の改善が期待されます。
症状が強い場合や効果が不十分な場合には、気管支拡張薬(β2刺激薬)を併用します。代表的な薬には、シムビコート®やレルベア®、フルティフォーム®などがあり、これらは吸入ステロイドと拡張薬が1つになった合剤であり、治療の継続がしやすい点が特徴です。
また、アレルギー体質が背景にある方には、抗アレルギー薬(抗ヒスタミン薬やロイコトリエン受容体拮抗薬など)の併用が有効です。アレルゲンへの反応を抑えることで咳の誘発を防ぎ、より安定したコントロールを目指すことができます。
感染後咳嗽(かんせんごがいそう)
- ・風邪などの感染症の後、2〜8週間続く咳
- ・他の明らかな疾患が見つからない
治療法:
-
感染後の咳(感染後咳嗽)は、風邪や気道感染の治癒後にも咳だけが長引くことが特徴で、2~8週間程度続くことがあります。ウイルス感染などによる気道の一時的な炎症や過敏性が原因と考えられています。
治療には、漢方薬、鎮咳薬が用いられます。代表的なものに麦門冬湯(ばくもんどうとう)、竹茹温胆湯(ちくじょうんたんとう)があります。
アトピー咳嗽
・ダニ・ハウスダスト・花粉などの吸入アレルゲンで誘発
治療法:
-
アトピー咳嗽は、ハウスダストやダニ、花粉などの吸入アレルゲンが原因で気道にアレルギー反応を起こし、咳が持続する疾患です。
治療の基本は、アレルギー反応を抑える薬物療法です。まず、第2世代抗ヒスタミン薬(例:アレグラ®、クラリチン®、デザレックス®など)が用いられ、くしゃみや鼻水といった他のアレルギー症状にも効果があります。
さらに、気道の炎症を抑える目的で、ロイコトリエン受容体拮抗薬(LTRA)も併用されることがあります。代表的な薬には、モンテルカストがあり、咳の頻度や重症度の軽減に役立ちます。
薬物治療に加えて、アレルゲンを取り除く生活環境の見直しも非常に重要です。布団・カーペットのこまめな掃除、空気清浄機の活用、寝具の防ダニカバーの使用など、日常生活の工夫が症状改善に大きく貢献します。
気管支喘息(きかんしぜんそく)
- ・呼吸困難、喘鳴(ゼーゼー)、夜間〜早朝の咳が特徴
- ・気道の慢性的な炎症と可逆性の気道閉塞
治療法:
-
気管支喘息は、気道の慢性的な炎症により、咳や喘鳴(ゼーゼーする音)、呼吸困難などが繰り返し起こる疾患です。治療の基本は、発作と呼吸機能低下を予防するための長期的な管理(コントロール)と、発作が起きた際の迅速な対応の2本柱です。
まず、長期管理薬(コントローラー)としては、吸入ステロイド薬(ICS)が最も重要です。代表的な薬剤にはアニュイティ®、パルミコート®、オルベスコ®などがあり、毎日継続的に使用することで気道の炎症を抑え、発作を予防します。
症状が中等度以上の場合には、ICSに長時間作用型β2刺激薬(LABA)を組み合わせた合剤(ICS+LABA)を使用します。代表的な薬剤にはシムビコート®やレルベア®、フルティフォーム®などがあり、炎症の抑制と気管支拡張の両方の効果が得られます。
また、アレルギーが関与している患者さんには、ロイコトリエン受容体拮抗薬(LTRA)も有効です。中でもモンテルカストは気道のアレルギー性炎症を抑える効果があり、内服薬として継続しやすいのが特徴です。
一方で、急な発作が起きた場合には、発作時の頓用薬(リリーバー)として吸入β2刺激薬(例:メプチン®吸入)を使用します。これにより気道が素早く広がり、呼吸の苦しさを和らげます。
なお、これらの治療でもコントロールが難しい重症喘息の患者さんには、専門施設での生物学的製剤(バイオ製剤)による治療が選択されることがあります。現在、日本で使用可能なバイオ製剤にはゾレア®(抗IgE抗体)、ヌーカラ®やファセンラ®(抗IL-5抗体)などがあり、患者さんの体質や症状に応じて使用されます。
COPD(慢性閉塞性肺疾患)
- ・喫煙歴がある高齢者に多い
- ・労作時の息切れ・慢性的な咳・痰が続く
治療法:
-
COPD(慢性閉塞性肺疾患)は、主に長年の喫煙などが原因で気道に慢性的な炎症や閉塞が生じ、咳・痰・息切れが徐々に進行していく呼吸器疾患です。治療の目的は、症状の進行を抑え、呼吸機能を保ちながら生活の質を維持することにあります。
治療の中心となるのは、吸入による気管支拡張薬の使用です。
-
LABA(長時間作用型β2刺激薬)は、気管支を広げる作用があり、呼吸を楽にします。代表的な薬剤にはオンブレス®吸入があります。
-
LAMA(長時間作用型抗コリン薬)は、気管支平滑筋を弛緩させ、呼吸抵抗を軽減します。主な薬にはスピリーバ®やエンクラッセ®が挙げられます。
-
症状が強い場合には、これら2種類を組み合わせたLABA+LAMA合剤が使われます。ウルティブロ®やアノーロ®、スピオルト®が代表的で、1日1回の吸入で効果が持続するため、継続しやすいのが利点です。
加えて、治療では禁煙の徹底が何より重要です。喫煙を続ける限り、症状の進行は止まりません。
また、呼吸リハビリテーション(息切れを軽減する呼吸法の指導や運動療法)を取り入れることで、日常生活の動作がより楽になります。
さらに、COPDは肺炎やインフルエンザに罹患すると重症化しやすいため、肺炎球菌ワクチンやインフルエンザワクチンなどの定期的な予防接種も欠かせません。
-
アレルギー性鼻炎・花粉症
- ・くしゃみ、鼻水、鼻づまり、目のかゆみ
- ・スギ花粉、ダニ、ハウスダストなどが原因
治療法:
-
アレルギー性鼻炎や花粉症は、鼻水・くしゃみ・鼻づまりに加え、咳や喉の違和感、さらには喘息悪化の引き金となることもある、非常に身近で影響の大きいアレルギー疾患です。
治療の基本は、アレルギー反応を抑える薬物療法です。
まず、抗ヒスタミン薬(内服薬)は、アレルギー症状を和らげる第一選択薬です。眠気の少ない第2世代抗ヒスタミン薬としては、アレグラ®、クラリチン®、ビラノア®などがあり、日常生活に支障なく服用できる点が大きな特徴です。
また、アレルギー性炎症を抑えるロイコトリエン受容体拮抗薬も併用されることがあり、特に咳や喘息症状を伴う場合に効果的です。代表的な薬にはモンテルカストがあります。
さらに、点鼻ステロイド薬は鼻の炎症や鼻づまりに対して非常に高い効果があり、ナゾネックス®やアラミスト®などがよく使われます。継続使用により、症状のピーク時期でも快適な生活が可能になります。
また、根本治療として注目されている「舌下免疫療法」も効果的です。これは、アレルゲンを少しずつ体に慣らすことで、体質そのものの改善を目指す治療法です。
おきのメディカルクリニックで行っている主な検査内容
呼吸器症状の原因を正確に診断するために、当院では以下の検査を実施しています。
呼吸機能検査(スパイロメトリー)
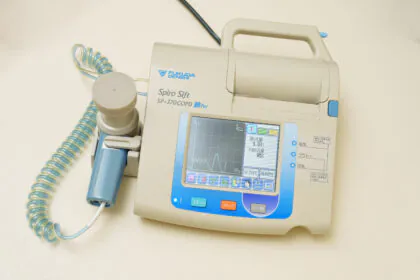 スパイロメトリーは、患者さまの肺の働きを客観的に数値で評価する検査です。息を深く吸い込み、できるだけ速く長く息を吐くことで、肺の空気の出入りの状態を測定します。この検査により、気道の狭窄や閉塞の有無を判断し、喘息や慢性閉塞性肺疾患(COPD)の診断や重症度の評価に役立ちます。検査は非侵襲的で、痛みもなく数分で終了します。
スパイロメトリーは、患者さまの肺の働きを客観的に数値で評価する検査です。息を深く吸い込み、できるだけ速く長く息を吐くことで、肺の空気の出入りの状態を測定します。この検査により、気道の狭窄や閉塞の有無を判断し、喘息や慢性閉塞性肺疾患(COPD)の診断や重症度の評価に役立ちます。検査は非侵襲的で、痛みもなく数分で終了します。
胸部X線検査
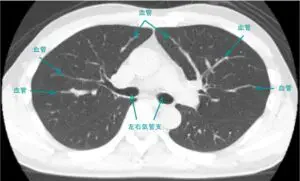
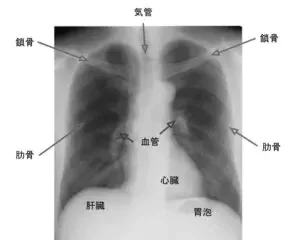 胸部X線(レントゲン)は、肺や胸郭の状態を画像で確認する検査です。肺炎や肺結核のような感染症のほか、間質性肺炎や肺がんなどの肺の構造的な異常を早期に発見できます。また、心臓の大きさや胸水の有無も評価できるため、呼吸器症状の原因を総合的に調べる際に欠かせません。
胸部X線(レントゲン)は、肺や胸郭の状態を画像で確認する検査です。肺炎や肺結核のような感染症のほか、間質性肺炎や肺がんなどの肺の構造的な異常を早期に発見できます。また、心臓の大きさや胸水の有無も評価できるため、呼吸器症状の原因を総合的に調べる際に欠かせません。
血液検査・アレルギー検査

血液検査では、全身の炎症の有無や白血球の状態を調べます。アレルギー検査では、特にIgE抗体のレベルを測定し、患者さまがどのアレルゲンに反応しているかを特定します。一般的なアレルゲンには、花粉、ダニ、ハウスダスト、ペットの毛などがあり、これによりアレルギー性鼻炎や気管支喘息の原因を明らかにし、より適切な治療方針の決定に役立てます。
その他の検査
 必要に応じて、咳や痰の原因を調べるための喀痰培養検査を行います。これは、細菌やウイルスの有無を調べ、適切な抗菌薬の選択に役立ちます。また、流行時期にはインフルエンザ検査やコロナウイルス検査も実施し、感染症の診断に役立てています。
必要に応じて、咳や痰の原因を調べるための喀痰培養検査を行います。これは、細菌やウイルスの有無を調べ、適切な抗菌薬の選択に役立ちます。また、流行時期にはインフルエンザ検査やコロナウイルス検査も実施し、感染症の診断に役立てています。
ご自宅でできる予防・対策のポイント(医師推奨)
-
呼吸器の症状を悪化させないためには、生活環境の整備が非常に重要です。特に乾燥しやすい冬季は、空気中の湿度が下がることで気道が刺激されやすくなり、咳や喉の不快感が増すことがあります。室内の湿度を40〜60%に保つことで、気道の乾燥を防ぎ、呼吸が楽になる方が多いです。また、アレルギーの原因となるホコリや花粉を減らすために、空気清浄機の活用もおすすめしています。
さらに、ホコリやダニの温床となる布団やカーテン、エアコンのフィルターは、定期的な掃除や洗濯を心がけましょう。これにより、アレルゲンの蓄積を防ぎ、症状の悪化を抑えることができます。
花粉の飛散が多い時期には、外干しした洗濯物に花粉が付着しやすいため、洗濯物は室内で干すことが望ましいです。外出時は、花粉の侵入を防ぐためにマスクやメガネを着用することも、症状の予防に役立ちます。
なお、市販の咳止め薬を自己判断で長期間続けるのは避けてください。咳は体が異物を排除しようとする自然な反応であり、症状の裏に重大な病気が隠れていることもあります。長引く咳や強い咳が続く場合は、必ず医師に相談し、適切な診断と治療を受けることが大切です。
-

咳や呼吸器症状が気になる方へ
咳が長引いている、風邪薬が効かない、毎年同じ時期に症状が出る……。
そんなときは、内科や呼吸器内科の専門的な診察が必要です。
おきのメディカルクリニック(宮城県仙台市若林区)では、地域に根ざした呼吸器疾患の診療を行っております。
経験豊富な医師が、丁寧な問診と検査に基づいて、患者様一人ひとりに最適な治療をご提案します。
クリニック情報・アクセス
-
【クリニック名】おきのメディカルクリニック
-
【診療科目】内科・呼吸器内科
-
【所在地】宮城県仙台市若林区沖野5丁目7-6
-
【Web予約】https://wakumy.lyd.inc/clinic/hg07051
-
【電話番号】022-352-3126








 ♦作り方♦
♦作り方♦


 ◆作り方
◆作り方




 以下、本文要旨の翻訳です。
以下、本文要旨の翻訳です。